10 ژانویه 2017 /دانشگاه تونگجی، موسسه ماتریا مدیکا شانگهای، آکادمی علوم چین و غیره / گزارش سلول های بنیادی
متن/ وو تین یائو
می توان گفت: «فراموش کن که کی هستی و من کی هستم» معمولی ترین علامت بیماری آلزایمر است.دلیل فراموشی یا ناتوانی در به خاطر سپردن وقایع اخیر این است که سلول های عصبی مسئول عملکردهای شناختی با گذشت سال ها ذره ذره می میرند، که باعث می شود بزرگسالانشناختی مرحلهبه انحطاط ادامه دهد
دانشمندان در مواجهه با این بیماری آلزایمر که به طور فزاینده ای شایع می شود، سخت کار می کنند تا درمان های عملی را مطالعه کنند.برخی از افراد بر مقصری که باعث مرگ سلول های عصبی می شود تمرکز می کنند و سعی می کنند تولید پروتئین بتا آمیلوئید را کاهش دهند.دیگران متعهد به ترویج بازسازی سلول های عصبی هستند، به این امید که جای خالی آسیب سلول های عصبی را جبران کنند، که شاید مفهوم "در صورت عدم وجود آن جبران شود".
در مغز پستانداران بالغ، در واقع دو ناحیه وجود دارد که به تولید سلول های عصبی جدید ادامه می دهند، یکی از آنها در شکنج هیپوکامپ است.این سلولهای عصبی خود تکثیر شونده «سلولهای پیشساز عصبی» نامیده میشوند.سلول هایی که به تازگی از آنها متولد شده اند به مدارهای عصبی اصلی اضافه می شوند تا به یادگیری مهارت های جدید و ایجاد خاطرات جدید کمک کنند.
با این حال، می توان در انسان یا موش مشاهده کرد که بیماری آلزایمر می تواند تکثیر سلول های پیش ساز عصبی را مختل کند.امروزه، شواهد بیشتر و بیشتری نشان می دهد که ترویج تکثیر سلول های پیش ساز عصبی می تواند زوال شناختی ناشی از بیماری آلزایمر را کاهش دهد و ممکن است به یک استراتژی عملی برای درمان بیماری آلزایمر تبدیل شود.
در ژانویه 2017، مطالعه ای که به طور مشترک در "گزارش های سلول های بنیادی" توسط دانشگاه تونگجی، موسسات علوم زیستی شانگهای، آکادمی علوم چین و غیره منتشر شد، ثابت کرد که پلی ساکاریدها یا عصاره های آب ازگانودرما لوسیدوم (قارچ Reishi، Lingzhi) می تواند اختلالات شناختی ناشی از بیماری آلزایمر را کاهش دهد، رسوب آمیلوئید β (Aβ) را در مغز کاهش دهد، و بازسازی سلول های پیش ساز عصبی در شکنج هیپوکامپ را تقویت کند.مکانیسم اثر دوم احتمالاً مربوط به فعال شدن گیرنده ای به نام FGFR1 بر روی سلول های پیش ساز عصبی به دلیل تنظیمگانودرما لوسیدوم.
موش های آلزایمر که غذا می خورندگانودرما لوسیدومحافظه بهتری دارند
در آزمایشهای حیوانی در این مطالعه از موشهای تراریخته APP/PS1 5 تا 6 ماهه استفاده شد - یعنی استفاده از فناوری انتقال ژن برای انتقال ژنهای انسانی جهش یافته APP و PS1 (که میتواند بیماری آلزایمر زودرس ارثی را القا کند) موش های تازه متولد شده برای بیان موثر ژن ها.این امر باعث می شود که مغز موش ها از سنین جوانی (پس از 2 ماهگی) شروع به تولید آمیلوئید β (Aβ) کند و وقتی به 5 تا 6 ماهگی رسیدند، به تدریج در تشخیص و حافظه فضایی با مشکل مواجه می شوند. .
به عبارت دیگر، موش های مورد استفاده در این آزمایش از قبل علائم اولیه بیماری آلزایمر را داشتند.محققان به موش های آلزایمری با GLP (پلی ساکاریدهای خالص جدا شده ازگانودرما لوسیدومپودر اسپور با وزن مولکولی 15 کیلو دالتون) با دوز روزانه 30 میلی گرم بر کیلوگرم (یعنی 30 میلی گرم به ازای هر کیلوگرم وزن بدن در روز) به مدت 90 روز متوالی.
سپس، محققان 12 روز دیگر را صرف آزمایش تواناییهای شناختی موشها در ماز آبی موریس (MWM) کردند و آنها را با موشهای مبتلا به بیماری آلزایمر که هیچگونه درمان پزشکی دریافت نکرده بودند و با موشهای معمولی مقایسه کردند.
موش ها نسبت به آب بیزاری طبیعی دارند.وقتی آنها را در آب قرار می دهند، سعی می کنند مکانی خشک برای استراحت پیدا کنند."تست ماز آبی موریس" از ماهیت آنها برای ایجاد یک سکوی استراحت در یک مکان ثابت در یک استخر بزرگ مدور استفاده می کند.از آنجایی که سکو زیر آب پنهان است، موش ها باید آن را تنها با یادگیری و به خاطر سپردن پیدا کنند.در نتیجه، محققان میتوانند بر اساس زمانی که موشها سکو را پیدا کردند، مسافتی که شنا کردند و مسیری که طی کردند، احمقتر یا باهوشتر شدن موشها قضاوت کنند.
مشخص شد که تفاوت معنی داری در سرعت شنای موش ها در هر گروه وجود ندارد.اما در مقایسه با موشهای معمولی، موشهای آلزایمر که هیچ درمانی دریافت نکرده بودند، مجبور بودند زمان بیشتری را صرف کنند و مسافتهای طولانیتری را شنا کنند تا سکو را در مسیری بینظم پیدا کنند که گویی از شانس برخوردار بودند، که نشان میدهد حافظه فضایی آنها به طور قابل توجهی مختل شده است.
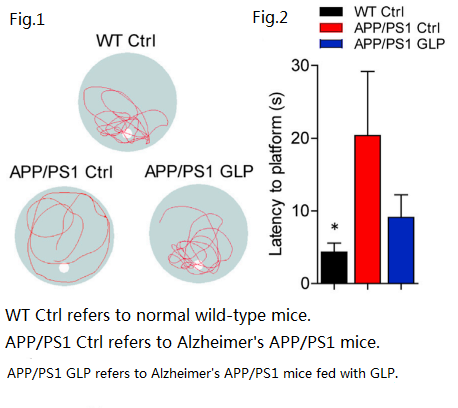
در مقابل، موش های آلزایمر که باقارچ ریشیپلی ساکاریدها یاگانودرما لوسیدومعصاره آب سکو را سریعتر پیدا کرد و قبل از یافتن سکو، عمدتاً در منطقه (ربع) که سکو قرار داشت، سرگردان بودند، گویی محل تقریبی سکو را می دانستند، که نشان می دهد آسیب به مغز آنها کمتر جدی است.【شکل 1، شکل 2】
علاوه بر این، محققان همچنین در آزمایش دیگری مشاهده کردند که برای مگسهای میوه که مقدار زیادی آمیلوئید β (Aβ) در مغزشان تولید میکنند (همچنین از طریق روشهای انتقال ژن برای ایجاد مدلهای تجربی)،گانودرما لوسیدومعصاره آب نه تنها می تواند توانایی های تشخیص فضایی و حافظه مگس میوه را بهبود بخشد، بلکه طول عمر مگس میوه را نیز افزایش می دهد.
محققان نیز استفاده کردندگانودرما لوسیدومعصاره آب (300mg/kg در روز) در آزمایشات حیوانی فوق الذکر نشان داد که می تواند اختلالات شناختی فضایی ناشی از بیماری آلزایمر را نیز مانند موارد فوق الذکر کاهش دهد.گانودرما لوسیدومپلی ساکاریدها (GLP).
از "تست ماز آبی موریس" برای ارزیابی توانایی حافظه فضایی موش ها استفاده کنید
[شکل 1] مسیرهای شنای موش ها در هر گروه.آبی استخر، سفید موقعیت سکو و قرمز مسیر شنا است.
[شکل 2] میانگین زمان لازم برای هر گروه از موش ها برای یافتن سکوی استراحت در روز هفتم آزمایش ماز آبی موریس
(منبع/گزارش های سلول های بنیادی. 2017 ژانویه 10; 8 (1): 84-94.)
لینگژیتکثیر سلول های پیش ساز عصبی در شکنج هیپوکامپ را ترویج می کند.
پس از آزمایش 12 روزه ماز آبی، محققان مغز موش ها را تجزیه و تحلیل کردند و متوجه شدندگانودرما لوسیدومپلی ساکاریدها وگانودرما لوسیدومعصاره های آب هم بازسازی سلول های عصبی در شکنج هیپوکامپ را تقویت می کنند و هم رسوب آمیلوئید β را کاهش می دهند.
همچنین تأیید شد که سلول های عصبی تازه متولد شده در شکنج هیپوکامپ عمدتاً سلول های پیش ساز عصبی هستند.وگانودرما لوسیدومبرای موش های مبتلا به آلزایمر موثر است.تغذیه موش های بالغ جوان عادی باگانودرما لوسیدومپلی ساکاریدها (GLP) با دوز روزانه 30 میلی گرم بر کیلوگرم به مدت 14 روز نیز می توانند تکثیر سلول های پیش ساز عصبی در شکنج هیپوکامپ را افزایش دهند.
آزمایشهای آزمایشگاهی همچنین تأیید کردهاند که برای سلولهای پیشساز عصبی جدا شده از شکنج هیپوکامپ موشهای بالغ سالم یا موشهای آلزایمر یا سلولهای پیشساز عصبی مشتقشده از سلولهای بنیادی انسانی،گانودرما لوسیدومپلی ساکاریدها می توانند به طور موثری این سلول های پیش ساز را به تکثیر تشویق کنند و سلول های تازه تولید شده ویژگی های اصلی سلول های پیش ساز عصبی را حفظ می کنند، یعنی می توانند تکثیر و خود نوسازی را انجام دهند.
تجزیه و تحلیل بیشتر نشان داد کهگانودرما لوسیدومپلی ساکاریدها (GLP) عمدتاً می توانند نوروژنز را تقویت کنند زیرا می توانند گیرنده ای به نام "FGFR1" (نه گیرنده EGFR) را بر روی سلول های پیش ساز عصبی تقویت کنند و آن را در برابر تحریک "عامل رشد عصبی bFGF" که اطلاعات بیشتری از "سلول" ارسال می کند حساس تر می کند. تکثیر» به سلول های پیش ساز عصبی، و سپس سلول های عصبی جدید بیشتری متولد می شوند.
از آنجایی که سلولهای عصبی تازه متولد شده میتوانند به مدارهای عصبی موجود بپیوندند تا پس از مهاجرت به ناحیه مغزی که به آن نیاز دارد، فعالیت کنند، این امر باید طیفی از اختلالات شناختی ناشی از مرگ سلولهای عصبی در بیماری آلزایمر را کاهش دهد.
نقش چند وجهی ازگانودرما لوسیدومسرعت فراموشی را کاهش می دهد
نتایج تحقیقات فوق به ما اجازه می دهد تا اثر محافظتی را ببینیمگانودرما لوسیدومروی سلول های عصبیعلاوه بر اثرات ضد التهابی، آنتی اکسیدانی، ضد آپوپتوز، رسوب ضد بتا آمیلوئید و سایر اثرات شناخته شده در گذشته،گانودرمالوسیدومهمچنین می تواند نوروژنز را تقویت کند.برای موشهای آلزایمر که نقصهای ژنتیکی یکسانی دارند و علائم مشابهی دارند، به همین دلیل است که شدت علائم بیماری بین موشهایی که غذا میخورند متفاوت است.گانودرما لوسیدومو کسانی که غذا نمی خورندگانودرما لوسیدوم.
گانودرما لوسیدومممکن است نتواند به طور کامل عملکرد حافظه را در بیماران آلزایمر بازگرداند، اما مکانیسم های مختلف اثر آن می تواند وخامت بیماری آلزایمر را کاهش دهد.تا زمانی که بیمار تا پایان عمر خود و دیگران را به یاد می آورد، بیماری آلزایمر ممکن است چندان وحشتناک نباشد.
[منبع] هوانگ اس، و همکاران.پلی ساکاریدهای گانودرما لوسیدوم عملکرد شناختی و تکثیر پیش ساز عصبی را در مدل موش بیماری آلزایمر تقویت می کنند.گزارش های سلول های بنیادی2017 ژانویه 10; 8 (1): 84-94.doi: 10.1016/j.stemcr.2016.12.007.
پایان
درباره نویسنده/ خانم وو تینگیائو
وو تینگیائو از سال 1999 اطلاعات دست اول گانودرما را گزارش کرده است. او نویسنده کتابدرمان با گانودرما(منتشر شده در The People's Medical Publishing House در آوریل 2017).
★ این مقاله با مجوز انحصاری نویسنده منتشر شده است.★ آثار فوق را نمی توان بدون مجوز نویسنده تکثیر، گزیده یا به روش های دیگر استفاده کرد.★ در صورت تخلف از بیانیه فوق، نویسنده مسئولیت های قانونی مربوطه را پیگیری خواهد کرد.★ متن اصلی این مقاله توسط Wu Tingyao به زبان چینی نوشته شده و توسط Alfred Liu به انگلیسی ترجمه شده است.اگر بین ترجمه (انگلیسی) و اصل (چینی) مغایرت وجود داشته باشد، اصل چینی ارجحیت دارد.اگر خوانندگان سؤالی دارند، لطفاً با نویسنده اصلی، خانم وو تینگیائو تماس بگیرید.
زمان ارسال: دسامبر-30-2021