1月 20, 2017 / 広東省微生物研究所および広東省疾病管理予防センター / 民族薬理学ジャーナル
文/呉廷耀

ということは昔から認識されている事実であり、 マンネンタケ 多糖類は糖尿病の治療に役立ちます, しかし、それがどのように機能するかは、科学者がさらに知りたいと思っているトピックです.
早くも 2012, 広東省微生物研究所と広東省疾病管理予防センターは共同で、高分子量多糖類は、 (GLP) の熱水抽出物から抽出されたマンネンタケ 子実体はタイプに対して良好な血糖降下効果を持っています 2 糖尿病(T2D).
今, 彼らはさらに、GLP から 4 つの多糖類を単離しました。, そしてよりアクティブなF31に乗りました (約の分子量 15.9 kDa, 含む 15.1% タンパク質) より深い勉強のために, そして、複数の経路を通じて血糖を調節するだけでなく、肝臓を保護することもできることがわかりました。.
霊芝 多糖類は高血糖を軽減することができます.
6週間の動物実験で, そのタイプであることが分かりました 2 糖尿病マウス (マンネンタケ グループ高用量) を与えた 50 mg/kgマンネンタケ 多糖類F31は毎日、未治療の糖尿病マウスよりも一貫して空腹時血糖値が低かった (対照群), そして大きな違いがありました.
対照的に, 糖尿病のマウス(マンネンタケ グループ低用量) それも食べたマンネンタケ 多糖類 F31 を毎日、ただし摂取量は 1 回のみ 25 mg/kg では血糖値の低下がそれほど顕著ではありませんでした. これは、マンネンタケ 多糖類には血糖値を調整する効果がある, ただし、効果は投与量によって影響されます (形 1).
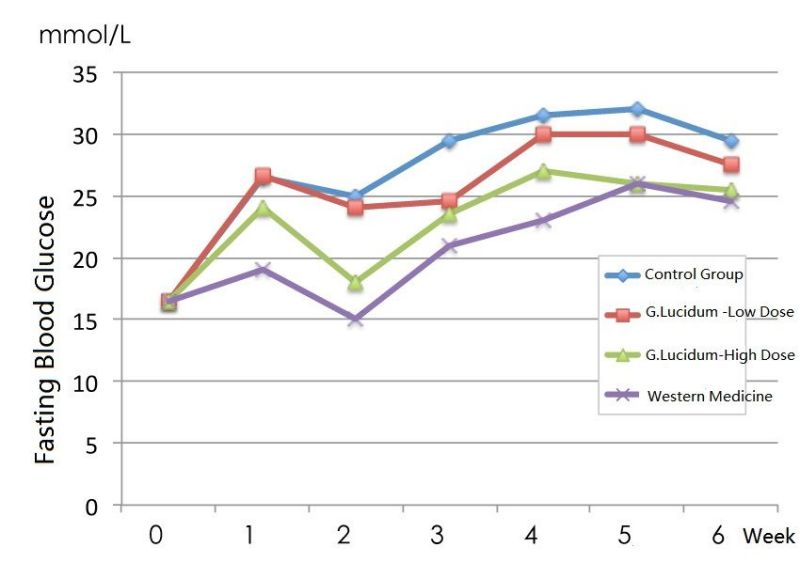
形 1 の効果マンネンタケ 糖尿病マウスの空腹時血糖値の研究
[説明] 「西洋医学グループ」で使用している血糖降下薬はメトホルミンです (ロディトン), 経口摂取されるもの 50 毎日mg/kg. 図中の血糖単位はmmol/Lです. 血糖値を次で割ります。 0.0555 mg/dLを取得するには. 正常な空腹時血糖値は以下である必要があります 5.6 ミリモル/L (約 100 mg/dL), より多い 7 ミリモル/L (126 mg/dL) 糖尿病です. (作画/呉廷耀, データソース/J Ethnopharmacol. 2017; 196:47-57.)
霊芝 多糖類は糖尿病による肝臓の損傷を軽減します.
図からわかります 1 それにもかかわらずマンネンタケ 多糖類F31は血糖を調節することができます, 効果は西洋薬より若干劣る, そして血糖値を正常に戻すことはできません. それにもかかわらず, マンネンタケ多糖類は肝臓を保護する役割を果たし始めています.
図からわかります 2, 実験中, によって保護されている糖尿病マウスの肝臓組織の構造と形態マンネンタケ 多糖類 F31 (50 mg/kg) 通常のマウスと同様でした, そして炎症も減りました. 対照的に, 何も治療を受けなかった糖尿病マウスの肝臓組織は著しく損傷していた, そして炎症と壊死の状態もさらに深刻でした。
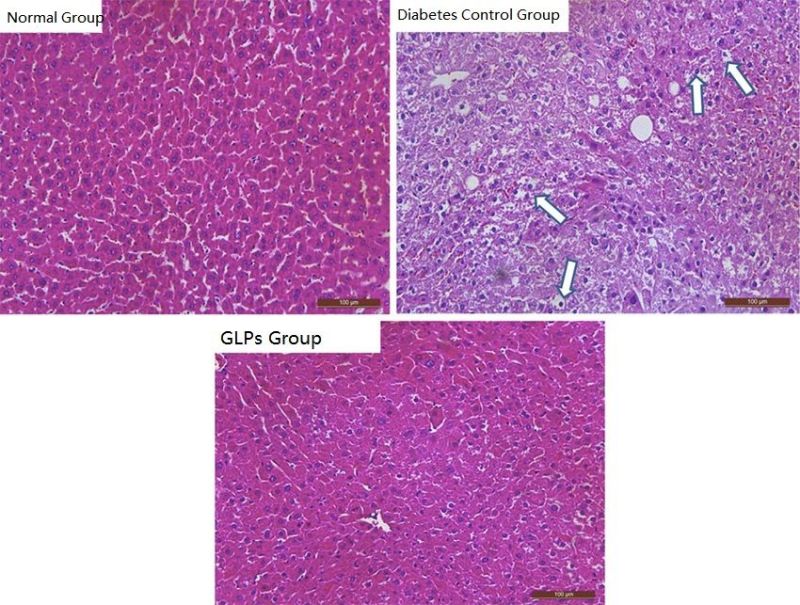
形 2 肝保護効果マンネンタケ糖尿病マウスの多糖類
[説明] 白い矢印は炎症または壊死性病変を示しています. (出典/J Ethnopharmacol. 2017; 196:47-57.)
タイプの発症 2 糖尿病
過去の多くの研究でそのメカニズムが説明されています。マンネンタケ 「膵島細胞を保護し、インスリン分泌を促進する」という観点から血糖を調節する多糖類。この研究は次のことを示唆していますマンネンタケ 多糖類は他の方法でも高血糖を改善します.
さらに進む前に, まず、活字を形成するためのいくつかの鍵を知る必要があります 2 糖尿病. 代謝機能が正常な人が食事をした後, 彼の膵島細胞はインスリンを分泌します, 筋肉細胞と脂肪細胞を刺激して「グルコーストランスポーター」を生成します。 (GLUT4)」が細胞表面に存在し、血液中のグルコースを細胞内に「輸送」します。.
ブドウ糖は細胞膜を直接通過できないため、, GLUT4の助けがなければ細胞に入ることができません。タイプの核心 2 糖尿病とは、細胞がインスリンに感受性を持たないことです (インスリン抵抗性). インスリンが頻繁に分泌されていても、, まだ細胞表面に十分なGLUT4を生成できません.
この状況は肥満の人に起こりやすい, 脂肪は「レジスチン」と呼ばれるペプチドホルモンを合成するためです。, 脂肪細胞のインスリン抵抗性を引き起こす.
ブドウ糖は細胞のエネルギー源なので、, 細胞がブドウ糖を欠いているとき, もっと食べたいと思わせるだけでなく、, また、肝臓がより多くのブドウ糖を生成するように促します.
肝臓がブドウ糖を生成するには2つの方法があります: 一つはグリコーゲンを分解すること, つまり, 肝臓に元々蓄えられていたブドウ糖を利用する; もう一つはグリコーゲンを再生することです, つまり, タンパク質や脂肪などの非炭水化物原料をブドウ糖に変換する.
タイプの患者におけるこれら 2 つの影響 2 糖尿病は普通の人に比べて重症度が高い. グルコース生成量が増加し続ける一方で、組織細胞によるグルコースの利用率が低下する場合, 血糖値は自然に下がりにくい.
マンネンタケ 多糖類は肝臓で生成されるグルコースの量を減らし、細胞によるグルコースの利用率を向上させます。.
マンネンタケ 多糖類F31は上記の問題を解決できると思われる. 動物実験終了後, 研究者らはマウスの肝臓と精巣上体の脂肪を取り出した (体脂肪の指標として), それらを分析して比較しました, F31には次のような作用機序があることが分かりました。 (形 3):
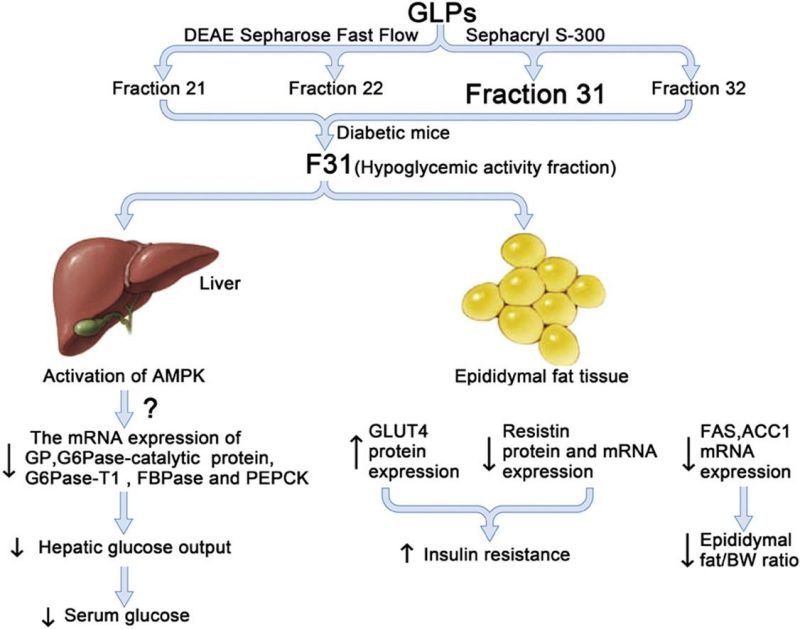
1.肝臓でAMPKプロテインキナーゼを活性化する, 肝臓におけるグリコーゲン分解または糖新生に関与するいくつかの酵素の遺伝子発現を低下させる, グルコース生成を減らす, 血糖値をソースからコントロールします.
2. 脂肪細胞上のGLUT4の数を増加させ、脂肪細胞からのレジスチンの分泌を阻害します。 (これら 2 つの変数を正常なマウスの状態に非常に近づけることにより、), それにより、インスリンに対する脂肪細胞の感受性が改善され、グルコースの利用が増加します。.
3. 脂肪組織における脂肪合成に関与する主要な酵素の遺伝子発現を大幅に減少させる, これにより、体重に占める脂肪の割合が減り、インスリン抵抗性に関連する要因が減少します。.
ことがわかりますマンネンタケ 多糖類は少なくとも 3 つの経路を通じて血糖を調節できる, そして、これらの経路は「インスリン分泌の刺激」とは何の関係もありません。, 糖尿病改善の可能性がさらに広がります。
形 3 の仕組みマンネンタケ 血糖調節における多糖類
[説明] 精巣上体は、精巣の上部に近いコイル状の細い精管です。, 精管と睾丸を接続する. 精巣上体周囲の脂肪は全身の脂肪と正の相関があるため、 (特に内臓脂肪), 実験の観察指標となることが多い. GPや他の酵素を減らす方法については、マンネンタケ 多糖類はAMPKを活性化します, さらに明確にする必要がある, したがって、2 つの関係は「」で示されます。?図中の「」. (出典/J Ethnopharmacol. 2017; 196:47-57.)
単一の種類のマンネンタケ 多糖類が必ずしも優れているわけではない.
上記の研究結果は、「どのようにしてマンネンタケ 多糖類はタイプに有益です 2 糖尿病". また、西洋医学を使用する初期段階では、マンネンタケ 多糖類, 血糖値は一度に正常に戻らないこともあり、図に示すように一定期間上下に変動することさえあります。 1.
この時点でがっかりしないでください, なぜなら食べている限りマンネンタケ, あなたの内臓は守られています.
言及する価値があるのは、, 記事の冒頭で述べたように, マンネンタケ 多糖類 F31 は、GLP から「分解された」小分子多糖類です。. 同じ実験条件下での血糖降下効果の比較, GLP の効果は F31 の効果よりも大幅に優れていることがわかります。 (形 4).
言い換えると, 単一の種類のマンネンタケ 多糖類が必ずしも優れているわけではない, しかし、包括的な種類の全体的な効果は、マンネンタケ 多糖類の方が大きい. GLPは、から得られる粗多糖類であるため、マンネンタケ 熱水抽出による子実体, を含む製品を食べる限り、マンネンタケ 子実体水抽出物, GLP を見逃すことはありません。
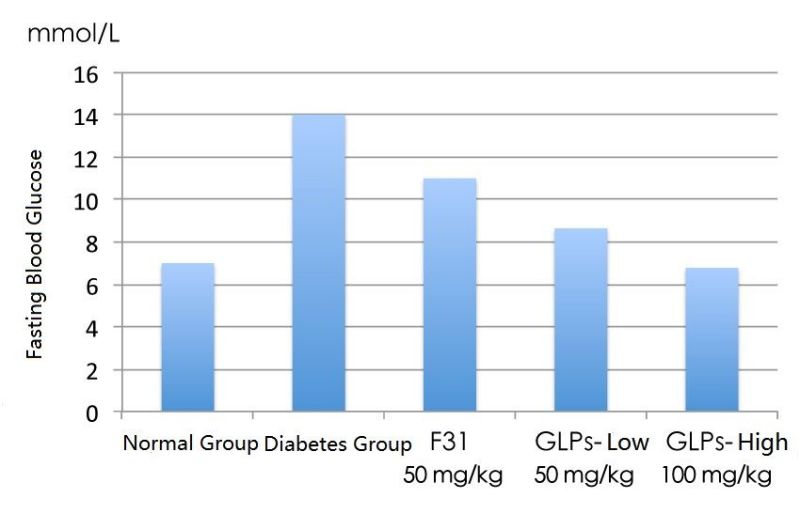
形 4 さまざまな種類の効果マンネンタケ 多糖類は空腹時血糖値に影響を与える
[説明] タイプ付きマウスの後 2 糖尿病 (空腹時血糖値 12-13 ミリモル/L) ~の腹腔内注射を毎日受けたマンネンタケ 多糖類 F31 (50 mg/kg), マンネンタケ 粗多糖類 GLP (50 mg/kg または 100 mg/kg) のために 7 連続した日々, 彼らの血糖値は、正常なマウスの血糖値および未治療の糖尿病マウスの血糖値と比較されました。. (作画/呉廷耀, データソース/Arch Pharm Res. 2012; 35(10):1793-801.J エスノファーマコール. 2017; 196:47-57.)
情報源
1. シャオC, 他. 糖尿病マウスにおける、霊芝多糖類 F31 の抗糖尿病活性が肝臓のグルコース調節酵素を下方制御する. J エスノファーマコール. 2017 1月 20;196:47-57.
2. シャオC, 他. マンネンタケ多糖類の血糖降下効果の種類 2 糖尿病マウス. アーチ製薬研究所. 2012 10月;35(10):1793-801.
終わり
著者について/Mさん. 呉廷耀
ウー・ティンヤオ氏は、以来、霊芝に関する直接の情報を報告し続けている。 1999. 彼女はの著者です霊芝による治癒 (4月に人民医学出版社に出版 2017).
★この記事は著者の独占的な許可を得て掲載されています.
★上記作品は転載禁止です, 著者の許可なく抜粋または他の方法で使用される.
★上記記載事項に違反した場合, 著者は関連する法的責任を追及します.
★この記事の原文はWu Tingyaoが中国語で執筆し、Alfred Liuが英語に翻訳しました。. 翻訳に齟齬があった場合 (英語) そしてオリジナル (中国語), 本来の中国人が勝つだろう. 読者に質問がある場合, 原作者に連絡してください, MS. 呉廷耀.



