Agosto 26, 2015 / Universidade Kyushu / Relatórios científicos
Texto/Wu Tingyao

A equipe de pesquisa de Kuniyoshi Shimizu, professor associado do Instituto de Ciências Agrícolas da Universidade de Kyushu, no Japão, confirmou que 31 triterpenóides isolados do corpo de frutificação de Ganoderma inibem a neuraminidase de cinco vírus influenza A em graus variados, entre os quais existem dois triterpenóides até adequados para desenvolvimento como medicamentos anti-influenza. Os resultados da pesquisa foram publicados em “Scientific Reports” do grupo editorial “Nature” no final de agosto. 2015.
A neuraminidase é uma das duas proteínas que se projetam na superfície dos vírus influenza A. Cada vírus influenza possui cerca de cem dessas proteases. Quando o vírus invade a célula e usa o material da célula para replicar novas partículas virais, a neuraminidase é necessária para que as novas partículas virais se separem da célula e infectem ainda mais outras células. Portanto, quando a neuraminidase perde sua atividade, o novo vírus ficará trancado na célula e não poderá escapar, a ameaça ao hospedeiro será reduzida, e a doença pode ser controlada. O oseltamivir comumente usado (Tamiflu) na prática clínica é usar este princípio para prevenir a proliferação e propagação do vírus.
De acordo com pesquisa realizada por Kuniyoshi Shimizu, numa concentração de 200 µM, esses triterpenóides Ganoderma inibiram a atividade do H1N1, H5N1, H7N9 e duas cepas mutantes resistentes NA (H1N1, N295S) e NA (H3N2, E119V) em graus variados. No geral, o efeito inibitório na neuraminidase do tipo N1 (especialmente H5N1) é o melhor, e o efeito inibitório sobre a neuraminidase do H7N9 é o pior. Entre esses triterpenóides, ganoderic acid TQ and ganoderic acid TR showed the highest levels of inhibition, and the effects of these two compounds ranged from 55.4% para 96.5% inibição para diferentes subtipos de NA.
Further analysis of the structure-activity relationship of these triterpenoids revealed that the triterpenoids, which have a better inhibitory effect on N1 neuraminidase, have the main structure of “tetracyclic triterpenoids with two double bonds, um ramo como um grupo carboxílico, e um grupo contendo oxigênio no sítio R5” (Backbone A na figura abaixo). Se a estrutura principal são as outras duas (Backbone B e C na figura abaixo), o efeito será ruim.
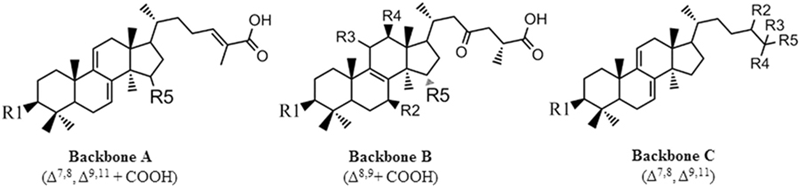
(Fonte/Representante Científico. 2015 AUG 26;5:13194.)
In silico docking is used to simulate the interaction of ganoderic acids (T-Q e TR) e neuraminidases (H1N1 e H5N1). Como resultado, descobriu-se que tanto os ácidos ganodéricos quanto o Tamiflu foram capazes de se ligar diretamente à área ativa da neuraminidase. Esta área ativa é composta por vários resíduos de aminoácidos. Os ácidos Ganoderma TQ e TR se ligarão aos dois resíduos de aminoácidos Arg292 e Glu119. Tamiflu tem outra opção, mas também pode tornar a neuraminidase ineficaz.
Comparado com a inibição de outras proteínas do vírus influenza (como a proteína M2, que abre a casca do vírus no momento em que o vírus se liga à célula hospedeira e envia os genes virais para a célula), os inibidores da neuraminidase são atualmente reconhecidos como medicamentos eficazes e menos resistentes para o tratamento da gripe. Portanto, os pesquisadores acreditam que os ácidos ganodéricos T-Q e TR, que são semelhantes, mas não iguais no mecanismo do Tamiflu, têm a oportunidade de serem usados como uma nova geração de medicamentos anti-influenza ou referências de design.
However, existe um pré-requisito para que o medicamento seja usado como medicamento anti-influenza, aquilo é, a droga deve inibir efetivamente a reprodução do vírus sem danificar as células infectadas pelo vírus. However, em experimentos em células infectadas com vírus vivos e linhagens celulares de câncer de mama (MCF-7), descobriu-se que quando os pesquisadores usaram esses dois tipos de ácidos ganodéricos sozinhos, eles tinham dúvidas sobre alta citotoxicidade, mas eles também encontraram outro tipo de triterpenóide Ganoderma, ganoderol B, tem um efeito inibitório sobre o H5N1 (mas o efeito inibitório é fraco), mas não é citotóxico. Portanto, os investigadores acreditam que a forma de melhorar a segurança dos ácidos ganodéricos T-Q e TR através da modificação da estrutura química, mantendo ao mesmo tempo a sua inibição da actividade da neuraminidase, deve ser cuidadosamente considerada.
[Fonte] Zhu Q, et al. Inhibition of neuraminidase by Ganoderma triterpenoids and implications for neuraminidase inhibitor design. Representante Científico. 2015 AUG 26;5:13194. doi: 10.1038/srep13194.
FIM
Sobre o autor/ ms. Wu Tingyao
Wu Tingyao tem relatado informações em primeira mão sobre Ganoderma desde 1999. Ela é autora de Cura com Ganoderma (Publicado na editora médica do povo em abril 2017).
★ Este artigo é publicado sob a autorização exclusiva do autor.
★ As obras acima não podem ser reproduzidas, extraído ou usado de outras formas sem a autorização do autor.
★ Por violações da declaração acima, o autor exercerá responsabilidades legais relevantes.
★ O texto original deste artigo foi escrito em chinês por Wu Tingyao e traduzido para o inglês por Alfred Liu. Se houver alguma discrepância entre a tradução (Inglês) e o original (chinês), o chinês original prevalecerá. Se os leitores tiverem alguma dúvida, entre em contato com o autor original, EM. Wu Tingyao.



